【みなとみらい IP Navigator】パテントリンケージにおける専門委員制度の運用フローについて
この記事の執筆者

弁理士 村松 大輔(プロフィールはこちら)
■専門分野
医薬品、再生医療、細胞培養、組み換えタンパク質、ペプチド製剤、核酸医薬、抗体医薬、細胞外小胞、遺伝子組み換え、遺伝子編集、PCR、次世代シーケンサー、DNA鑑定、バイオインフォマティクス、菌株、質量分析、イムノアッセイ、農業科学、化粧品、食品こんにちは。弁理士の村松です。
令和7年11月14日付で、厚生労働省より「医薬薬審発 1114 第1号」通知(以下、「本通知」といいます。)が発出され、医療用後発医薬品およびバイオ後続品の承認審査における専門委員制度の試行が正式に開始されました。私も厚生労働省の専門委員候補に選任されておりますが、本稿では、当該制度が適用された場合の実務上の運用フローについて、専門委員候補に向けて開催された事前説明会での質疑応答の内容なども踏まえ、企業の知財担当者が留意すべきポイントを中心に解説します。
なお、制度の全体像や背景については、10月23日付の記事「【みなとみらい IP Navigator】新しいパテントリンケージ制度の導入について」にて解説済みですので、そちらをご参照ください。
専門委員制度運用の全体フロー
本制度は、厚生労働省医薬局医薬品審査管理課(以下、「医薬品審査管理課」)が、承認申請中の品目を「対象品目」として指定することで開始されます。
運用の流れは大きく分けて、「指定・資料提出」、「専門委員の選定」、「審議・意見書作成」、「手続終了・開示」の4段階で進行します。運用フローの全体像を以下の模式図に示します。
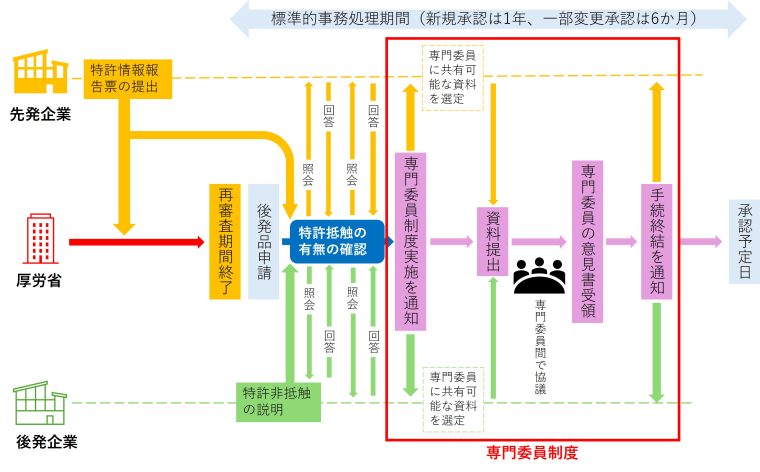
以下、各フェーズにおける実務対応の詳細を解説します。
1.対象品目の指定と資料提出(通知から30営業日以内)
医薬品審査管理課が特定の後発医薬品等を対象品目として指定すると、後発企業および先発企業双方にその旨が通知されます。
この通知を受けた企業は、以下の対応を求められます。まず、通知を受けた日から30営業日以内に、専門委員への共有について「同意する」資料を特定し、医薬品審査管理課へ提出する必要があります。
本通知によれば、提出可能な資料には以下が含まれます。- 承認申請資料(CTD1.4等)
- 医薬品特許情報報告票
- 特許抵触の有無に関する自社または特許権者の見解をまとめた資料
- 特許抵触の有無に関する専門家の意見書または鑑定書
- 判例や学説等の参考文献
- 特許庁による判定制度の結果
重要な点は、専門委員は当事者が同意した資料および公開情報(特許公報や添付文書等)のみに基づいて検討を行うという点です。
したがって、自社の主張を裏付けるために不可欠な資料については、確実に共有同意を行う必要があります。また、この期間に、厚生労働省のウェブサイトで公開されている「専門委員候補名簿」を確認し、自社と特別の利害関係(顧問契約や親族関係等)を有する候補者がいる場合は、医薬品審査管理課へ申告する必要があります。
2.専門委員の選定
医薬品審査管理課は、双方の企業から申告された利害関係情報を踏まえ、特別の利害関係がない専門委員(通常3名)を選定し、意見照会を行います。
なお、事前説明会での厚労省の回答によれば、検討対象となる特許は、あらかじめ厚労省が当事者に確認を実施し、特許番号まで特定した状態で専門委員に照会されることとなっています。
3.専門委員による検討と意見書の作成(目安:30営業日)
選定された専門委員は、提供された資料に基づき検討を行います。
直接的な文言侵害の有無(延長された特許権への抵触判断を含む)が検討対象であり、間接侵害や均等侵害は検討の対象外とされています。検討期間は、資料提供から30営業日以内を目処とされています。
ただし、事前説明会での厚労省の見解によれば、懸案特許の数が極端に多い場合や、追加照会に時間を要した場合等は、標準的事務処理期間等を鑑みて弾力的に期限設定を検討する余地があるとされています。この検討プロセスにおいて、専門委員は必要に応じて、医薬品審査管理課を介して当事者企業(後発企業または先発企業)に対し、質問や追加資料の提供依頼を行うことができます。
企業側は、この依頼に対して速やかかつ誠実に対応することが求められます。最終的に、専門委員は合議の上で連名による「意見書」を作成し、厚生労働省へ提出します。
意見書の結論は「特許抵触あり」または「特許抵触なし」のいずれかが示されます。
理由部分については、抵触の可能性の多寡や微妙なニュアンスを含めて記載されることもあり得ます。また、結論部分の意見が2:1で割れるケースがあった場合には、理由欄に反対意見が付記されることも許容されております。4.最終判断と意見書の開示
医薬品審査管理課は、提出された意見書の内容を参考に、特許抵触の有無について確認を行い、承認の可否を最終判断します。
あくまで最終判断の権限は厚生労働省にあり、専門委員の意見書は何ら法的拘束力を有しません。専門委員への意見照会手続が終了した段階で、その旨が企業へ通知されます。
その後、承認予定日の経過等により、承認可否の最終的な判断が公になった後、希望する企業に対して意見書の写しが開示されます。開示される意見書では、専門委員の氏名・所属はマスキング(黒塗り)されます。
また、第三者に開示することで企業の正当な利益を害するおそれがある情報についてもマスキングの対象となります。なお、開示された意見書の用途について、事前説明会では「当事者に委ねられている」とされており、理論上は訴訟資料として提出される事態もあり得ると回答されています。
実務上の留意点
本制度の導入により、先発企業・後発企業ともに、特許抵触に関する主張立証活動が、従来の厚生労働省との直接的なやり取りに加え、専門委員という第三者を意識したものへと変化します。
特に、専門委員への共有資料の選別や、追加質問への迅速な回答対応は、承認審査の行方を左右する重要な要素となります。知財担当者におかれましては、30営業日という限られた期間内で適切な資料を提出できるよう、事前の準備体制を整えておくことが推奨されます。
お気軽にご相談・お問い合せくださいませ
